LG München I, Urteil vom 20.11.2014, Az. 7 O 13161/14
§ 9 S. 2 Nr. 3 PatG
Das LG München I hat entschieden, dass auch für unkörperliche Gegenstände (hier: Genanalyse) ein sog. derivater Erzeugnisschutz gemäß § 9 Satz 2 Nr. 3 PatG bestehen kann. Notwendig sei allerdings, dass der unkörperliche Gegenstand verkehrsfähig sei, auf einem Speichermedium befindlich mehrfach benutzt werden könne und eine Prägung durch die erfindungswesentlichen Merkmale des geschützten Verfahrens. Reines Know-How, bei dem der Wert des Gegenstandes in der einmaligen Informationsübermittlung bestehe, sei hiervon ausgenommen. Zum Volltext der Entscheidung:
Landgericht München I
Urteil
…
I.
Die Klage wird abgewiesen.
II.
Die Klägerin hat die Kosten des Rechtsstreits zu tragen.
III.
Das Urteil ist gegen Sicherheitsleistung in Höhe von 110 % des jeweils vollstreckbaren Betrages vorläufig vollstreckbar.
Tatbestand
Die Klägerin macht gegen die Beklagten Ansprüche wegen behaupteter Patentverletzung geltend. Die Klage stützt sich auf das Patent … („Nukleinsäure, die für eine Rezeptor-Proteinkinase kodiert“). Eingetragene Inhaberin ist die T.
Das Klagepatent nimmt eine japanische Priorität vom 18. Oktober 1996 in Anspruch. Die Anmeldung erfolgte am 13.10.1997; der Hinweis auf die Erteilung wurde am 23. August 2006 veröffentlicht. Die deutsche Übersetzung des Klagepatents wurde am 23. August 2007 veröffentlicht.
Das Klagepatent betrifft u. a. eine Nukleinsäure, die eine Rezeptor-Proteinkinase codiert, welche eine Tandemverdopplung in einer Nukleotidsequenz einer Juxtamembran umfasst, sowie ein Verfahren zum Nachweis der vorstehend genannten Nukleinsäure.
Gegen das Klagepatent erhob die Beklagte zu 1) am 03.11.2011 Nichtigkeitsklage beim Bundespatentgericht, welche dort unter dem Aktenzeichen 3 NI 37/11 geführt wurde. Das Klagepatent wurde erstinstanzlich beschränkt aufrechterhalten. Das Nichtigkeitsverfahren befindet sich derzeit im Berufungsstadium vor dem Bundesgerichtshof (Az.: X ZR 141/13). Der hier geltende gemachte Anspruch 7 des Klagepatents wurde vom Bundespatentgericht als Anspruch 1 aufrechterhalten.
Der hier relevante Anspruch 1 des streitgegenständlichen Patents lautet in der vom BPatG aufrecht erhaltenen Form (die Abweichungen zur erteilten Fassung sind kenntlich gemacht):
Verfahren zum Nachweis eines Nukleinsäuremoleküls einer Tandemverdopplungsmutante, das humane FMS-artige Tyrosinkinase 3 (FLT3) codiert, wobei das Nukleinsäuremolekül eine Nucleotidsequenz hat entsprechend: einer Tandemverdopplungsmutation in der Nucleotidsequenz [einer Region umfassend] von Exon 11 oder Exons 11 bis 12 von FLT3 ohne Verschiebung des Leserasters, die durch Primer der SEQ ID No. 26 und SEQ ID NO: 27 amplifiziert werden kann und als Längenmutation nachweisbar ist, umfassend die Schritte:
a) Durchführung einer Genamplifikationsreaktion mit einer Nukleinsäureprobe von einem Menschen, wobei ein Nukleinsäurefragment, das Exon 11 oder Exons 11 bis 12 des FMS-artigen Tyrosinkinase 3 (FLT3)-Gens umfasst und eine Tandemverdopplungsmutation in der Juxtamembran hat, amplifiziert wird, welches im FLT3-Gen gefunden werden kann;
b) Nachweis der Anwesenheit der Tandemverdopplungsmutation in dem Nukleinsäurefragment aus Schritt a).
Anspruch 3 (bisher Anspruch 8), der durch das Urteil des BPatG vom 09.07.2013 nicht berührt wurde, lautet:
Verfahren nach Anspruch 1 oder 2, wobei Schritt (b) ausgeführt wird durch Vergleichen des amplifizierten Nukleinsäurefragments, erhalten in Schritt (a), mit einer Sequenz, die von einer normalen FLT3 abgeleitet ist, wobei auf diese Weise die Anwesenheit einer Tandemverdopplungsmutation in der Juxtamembran nachgewiesen wird.
Anspruch 4 (bisher Anspruch 9), der inhaltlich durch das Urteil des BPatG vom 09.07.2013 ebenfalls nicht verändert wurde, lautet:
Verfahren nach einem der Ansprüche 1 bis 3, wobei in Schritt (b) eine Längenmutation als Index für die Tandemverdopplungsmutation verwendet wird.
Die Klägerin ist eine Tochtergesellschaft der I… . Sie betreibt ein Diagnoselabor, welches Tests ausführt, die unter den Schutzbereich des Klagepatents fallen. In ihrer Bilanzsumme für 2011 von 397.110,22 € sind Verbindlichkeiten in Höhe von 388.970,22 € enthalten. Der nicht durch Eigenkapital gedeckte Fehlbetrag beläuft sich auf 50.134,31 €. Der Jahresabschluss für 2012 weist in der Bilanzsumme von 1.136.389,53 € Verbindlichkeiten in Höhe von 1.124.500,82 € auf; der nicht durch Eigenkapital gedeckte Fehlbetrag beläuft sich auf 534.696,94 €.
Ausschließliche Lizenznehmerin am Klagepatent … ist die I… . Diese ermächtigte die Klägerin, den der I… zustehenden Unterlassungsanspruch aus dem Klagepatent gegen die Beklagten geltend zu machen. Ferner trat die I… der Klägerin alle ihr zustehenden Rechte aus dem ausschließlichen Lizenzvertragsverhältnis am Klagepatent ab.
Die Beklagte zu 2) ist eine tschechische Gesellschaft, die wie die Beklagte zu 1) von den Beklagten zu 4) bis 7) als Geschäftsführer geführt wird.
Die Beklagte zu 3) ist eine von den Beklagten zu 4) bis 7) in Form einer Partnerschaftsgesellschaft geführte Gemeinschaftspraxis.
Die Beklagten zu 1) und zu 3) bieten auf ihren Internetseiten ein Untersuchungsformular für Genuntersuchungen zum Download an, auf welchem die Beklagten zu 1) und 3) gemeinsam im Briefkopf firmieren. Dort findet der Kunde die Anweisung, Proben an die Adresse der Beklagten zu 3) einzusenden. Die Internetseite der Beklagten zu 1) ist auf der Internetseite der Beklagten zu 3) verlinkt. Unter der Rubrik „Diagnostik“ wird auf der Internetseite der Beklagten zu 3) die enge Kooperation mit der Beklagten zu 1) weiter herausgestellt. Zwischen der Beklagten zu 3) und der Beklagten zu 2) besteht ein Kooperationsvertrag unter anderem zur Untersuchung von Patientenproben mittels dem streitgegenständlichen Verfahren im Ausland. Gemäß den Vorgaben dieses Vertrages hat die Beklagte zu 3) an die Beklagte zu 2) einmalig einen Betrag von € 20.000,- zu bezahlen sowie fortlaufend weitere € 15,- pro durchgeführtem Test.
Bei den Beklagten zu 3) bis 7) eingehende Patientenproben, bei denen der Einsender unter anderem eine FLT3-LM Untersuchung wünscht, werden dort wie folgt bearbeitet: Es findet eine Zellaufbereitung und eine Extraktion sämtlicher in den Proben enthaltener Nukleinsäuren statt, wie sie für molekulargenetische Untersuchungen im Allgemeinen durchgeführt wird. Dabei wird DNA aus den Zellen isoliert und es erfolgen eine enzymatische Transkription von RNA in DNA mittels reverser Transkriptase sowie eine Dichtengradientenisolierung von Zellen, Organellen und Proteinen. Ein Teil dieser zurückgestellten Nukleinsäuren wird an die Beklagte zu 2) in der Tschechischen Republik weitergeleitet. Die Beklagten entsenden dafür wöchentlich verschiedene Mitarbeiter der Beklagten zu 1) bzw. 3) zur Beklagten zu 2) nach Prag, damit diese dort die FLT3-ITD-Analyse vornehmen oder jedenfalls die dortigen Mitarbeiter dabei unterstützen. Eine spezifische Aufbereitung für die im patentfreien Ausland stattfindende Untersuchung auf eine Längenmutation in einem Abschnitt im FLT3-Gen findet in der Bundesrepublik Deutschland weder durch die Beklagte zu 1) noch durch die Beklagten zu 3) bis 7) statt.
Die Beklagte zu 2) führt die Untersuchung auf eine Längenmutation in einem Abschnitt im FLT3-Gen (FLT3-LM) in der Tschechischen Republik durch. Dabei wird untersucht, ob eine Längenmutation im FLT3-Gen vorhanden ist, und die sog. „Mutationslast“ bestimmt.
Die Beklagte zu 2) schickt nach vollbrachtem Test eine Kopie des Testberichts direkt an den Auftraggeber, der die Probe an die Beklagte zu 1) in München gesandt und ihr den Untersuchungsauftrag erteilt hat, sowie eine weitere Kopie des Testberichts an die Beklagten zu 1) und 3), damit diese den Bericht in ihrem EDV-System speichern.
Dabei rechnet keine der Beklagten die in Prag durchgeführten Untersuchungen ab. Lediglich die Beklagte zu 3) hat die im Kooperationsvertrag vereinbarten Gebühren an die Beklagte zu 2) bezahlt, welche der Deckung der laufenden Kosten der Beklagten zu 2) für Miete, Verbrauchsmittel, Personal etc., nicht aber der Gewinnerzielung dienen soll. Gegenüber den Patienten werden die in Deutschland erbrachten Leistungen berechnet, namentlich die Isolierung der DNA aus den Zellen, die enzymatische Transkription von RNA in DNA mittels reverser Transkriptase sowie die Dichtengradientenisolierung von Zellen, Organellen und Proteinen.
Es wird kein Probenmaterial von der Beklagten zu 2) an die Beklagte zu 1) oder die Beklagten zu 3) bis 7) zurückgesandt.
Die Kammer hat in dem Verfahren 7 O 17048/12 mit Entscheidung vom 25. April 2013 die Beklagten zu 1) und 4) bis 7) wegen Verletzung des Anspruchs 7 (in der erteilten Fassung) des deutschen Teils des Europäischen Patents … zu Unterlassung, Auskunft- und Rechnungslegung sowie Feststellung der Schadensersatzpflicht verurteilt.
Die Klägerin behauptet, die Beklagten zu 1) und zu 3) würden die streitgegenständliche Untersuchung in Deutschland anbieten. Die Beklagten könnten das Testergebnis zur weiteren Diagnose und Behandlung des Patienten ihrer Auftraggeber verwenden und würden in der Praxis tatsächlich auch so verfahren. Ziel der Beklagten sei es, der Klägerin maximal zu schaden. Die Klägerin ihrerseits könne einen potentiellen Kostenerstattungsanspruch der Beklagten infolge der Unterstützung durch ihre Muttergesellschaft befriedigen.
Die Klägerin meint, das Vorgehen der Beklagten sei als Patentverletzung gemäß § 9 S. 2 Nr. 3 PatG wegen Verwendung eines unmittelbaren Verfahrenserzeugnisses in Deutschland und/oder als Patentverletzung unter mittäterschaftlichen Gesichtspunkten gemäß § 9 S. 2 Nr. 2 PatG sowie als mittelbare Patentverletzung nach § 10 Abs. 1 PatG zu bewerten.
Die Klägerin beantragt:
Die Beklagten werden verurteilt,
I. es bei Meidung eines für jeden Fall der Zuwiderhandlung vom Gericht festzusetzenden Ordnungsgeldes bis zu € 250.000,00 – ersatzweise Ordnungshaft – oder einer Ordnungshaft bis zu 6 Monaten, im Falle wiederholter Zuwiderhandlung bis zu insgesamt 2 Jahren, wobei die Ordnungshaft hinsichtlich der Beklagten zu 1) bis 3) an ihren Geschäftsführern bzw. Partnern zu vollziehen ist, zu unterlassen,
Untersuchungsergebnisse, die unmittelbar gewonnen wurden aus einem Verfahren zum Nachweis eines Nukleinsäuremoleküls einer Tandemverdopplungsmutante, das humane FMS-artige Tyrosinkinase 3 (FLT3) codiert, wobei das Nukleinsäuremolekül eine Nucleotidsequenz hat entsprechend: einer Tandemverdopplungsmutation in der Nucleotidsequenz von Exon 11 oder Exons 11 bis 12 von FLT3 ohne Verschiebung des Leserasters, die durch Primer der SEQ ID NO: 26 und SEQ ID NO: 27 amplifiziert werden kann und als Längenmutation nachweisbar ist, umfassend die Schritte:
a) Durchführung einer Genamplifikationsreaktion mit einer Nukleinsäureprobe von einem Menschen, wobei ein Nukleinsäurefragment, das Exon 11 oder Exons 11 bis 12 des FMS-artigen Tyrosinkinase 3 (FLT3)-Gens umfasst und eine Tandemverdopplungsmutation in der Juxtamembran hat, amplifiziert wird, welches im FLT3-Gen gefunden werden kann;
b) Nachweis der Anwesenheit der Tandemverdopplungsmutation in dem Nukleinsäurefragment aus Schritt a),
unabhängig davon, ob und wie diese Untersuchungsergebnisse verkörpert wurden, in der Bundesrepublik Deutschland anzubieten, in Verkehr zu bringen oder zu gebrauchen oder zu den genannten Zwecken entweder einzuführen oder zu besitzen;
(Unmittelbare Verletzung des Anspruchs 1 des Klagepatents wie aufrechterhalten nach § 9 S. 2 Nr. 3 PatG)
II. es bei Meidung eines für jeden Fall der Zuwiderhandlung vom Gericht festzusetzenden Ordnungsgeldes bis zu € 250.000,00 – ersatzweise Ordnungshaft – oder einer Ordnungshaft bis zu 6 Monaten, im Falle wiederholter Zuwiderhandlung bis zu insgesamt 2 Jahren, wobei die Ordnungshaft hinsichtlich der Beklagten zu 1) bis 3) an ihren Geschäftsführern bzw. Partnern zu vollziehen ist,
zu unterlassen
Verfahren zum Nachweis eines Nukleinsäuremoleküls einer Tandemverdopplungsmutante, das humane FMS-artige Tyrosinkinase 3 (FLT3) codiert, wobei das Nukleinsäuremolekül eine Nucleotidsequenz hat entsprechend: einer Tandemverdopplungsmutation in der Nucleotidsequenz von Exon 11 oder Exons 11 bis 12 von FLT3 ohne Verschiebung des Leserasters, die durch Primer der SEQ ID NO: 26 und SEQ ID NO: 27 amplifiziert werden kann und als Längenmutation nachweisbar ist, umfassend die Schritte:
a) Durchführung einer Genamplifikationsreaktion mit einer Nukleinsäureprobe von einem Menschen, wobei ein Nukleinsäurefragment, das Exon 11 oder Exons 11 bis 12 des FMS-artigen Tyrosinkinase 3 (FLT3)-Gens umfasst und eine Tandemverdopplungsmutation in der Juxtamembran hat, amplifiziert wird, welches im FLT3-Gen gefunden werden kann;
b) Nachweis der Anwesenheit der Tandemverdopplungsmutation in dem Nukleinsäurefragment aus Schritt a).
im gegenseitigen Zusammenwirken der Beklagten zu 2) mit zumindest einer der Beklagten zu 1) und 3) bis 7) oder – für die Beklagten zu 1) und 3) bis 7) – auch im Zusammenwirken mit einem sonstigen im Ausland befindlichen Dritten anzuwenden oder zur Anwendung in der Bundesrepublik Deutschland anzubieten, wenn die Beklagten zu 1) und 3) bis 7) zumindest einen der Schritte „Isolation von DNA aus den Zellen“, „enzymatische Transkription von RNA in DNA mittels reverser Transkriptase“ oder „Dichtengradientenisolierung von Zellen, Organellen und Proteinen“ in der Bundesrepublik Deutschland und die Beklagte zu 2) oder ein sonstiger im Ausland befindlicher Dritter die Verfahrensschritte a) und b) des vorstehend genannten Patentanspruchs ausführen oder anbieten.
(Unmittelbare mittäterschaftliche Verletzung des Anspruchs 1 des Klagepatents wie aufrechterhalten nach § 9 S. 2 Nr. 2 PatG)
III. – nur für die Beklagten zu 1) und 3) sowie die Beklagten zu 4) bis 7) –
es bei Meidung eines für jeden Fall der Zuwiderhandlung vom Gericht festzusetzenden Ordnungsgeldes bis zu € 250.000,00 – ersatzweise Ordnungshaft – oder einer Ordnungshaft bis zu 6 Monaten, im Falle wiederholter Zuwiderhandlung bis zu insgesamt 2 Jahren, wobei die Ordnungshaft hinsichtlich der Beklagten zu 1) und 3) an ihren Geschäftsführern bzw. Partnern zu vollziehen ist,
zu unterlassen,
Patientenproben, die geeignet und bestimmt sind zur Verwendung in einem Verfahren zum Nachweis eines Nukleinsäuremoleküls einer Tandemverdopplungsmutante, das humane FMS-artige Tyrosinkinase 3 (FLT3) codiert, wobei das Nukleinsäuremolekül eine Nucleotidsequenz hat entsprechend: einer Tandemverdopplungsmutation in der Nucleotidsequenz von Exon 11 oder Exons 11 bis 12 von FLT3 ohne Verschiebung des Leserasters, die durch Primer der SEQ ID NO: 26 und SEQ ID NO: 27 amplifiziert werden kann und als Längenmutation nachweisbar ist, umfassend die Schritte:
a) Durchführung einer Genamplifikationsreaktion mit einer Nukleinsäureprobe von einem Menschen, wobei ein Nukleinsäurefragment, das Exon 11 oder Exons 11 bis 12 des FMS-artigen Tyrosinkinase 3 (FLT3)-Gens umfasst und eine Tandemverdopplungsmutation in der Juxtamembran hat, amplifiziert wird, welches im FLT3-Gen gefunden werden kann;
b) Nachweis der Anwesenheit der Tandemverdopplungsmutation in dem Nukleinsäurefragment aus Schritt a).
an Dritte zur Verwendung in dem vorgenannten Verfahren und anschließendem Import oder Inverkehrbringen des aus diesem Verfahren resultierenden Untersuchungsergebnisses in die/der Bundesrepublik Deutschland anzubieten oder zu liefern.
(Mittelbare Verletzung des Anspruchs 1 des Klagepatents wie aufrechterhalten nach § 10 Abs. 1 PatG)
IV. der Klägerin darüber Auskunft zu geben und Rechnung zu legen, in welchem Umfang die Beklagten die unter I., II. und III. (für Handlungen gemäß III. nur für die Beklagten zu 1) und 3) sowie die Beklagten zu 4) bis 7)) beschriebenen Handlungen seit dem 23. September 2006 begangen haben, und zwar unter Vorlage eines geordneten Verzeichnisses unter Beifügung der Belege, insbesondere unter Angabe
a) der einzelnen Leistungen, aufgeschlüsselt nach Leistungsmengen, -zeiten und -preisen unter Einschluss von Typenbezeichnungen sowie Namen und Anschriften der Abnehmer,
b) der einzelnen Angebote, aufgeschlüsselt nach Angebotsmengen, -zeiten und -preisen unter Einschluss von Typenbezeichnungen sowie Namen und Anschriften der Angebotsempfänger,
c) der betriebenen Werbung, aufgeschlüsselt nach Werbeträgern, deren Auflagenhöhe, Verbreitungszeitraum und Verbreitungsgebiet,
d) der nach den einzelnen Kostenfaktoren aufgeschlüsselten Gestehungskosten und des erzielten Gewinns,
wobei die zugehörigen Leistungsbelege (Rechnungen) mit der Maßgabe vorzulegen sind, dass Daten, auf die sich die geschuldete Auskunft und Rechnungslegung nicht bezieht und hinsichtlich derer ein berechtigtes Geheimhaltungsinteresse der Beklagten besteht, abgedeckt oder geschwärzt sein können, und wobei den Beklagten vorbehalten bleiben mag, die Namen und Anschriften der nichtgewerblichen Abnehmer und der Angebotsempfänger statt der Klägerin einem von dieser zu bezeichnenden und ihr gegenüber zur Verschwiegenheit verpflichteten vereidigten Wirtschaftsprüfer mitzuteilen, sofern die Beklagten dessen Kosten tragen und ihn ermächtigen und verpflichten, der Klägerin auf konkrete Nachfrage mitzuteilen, ob bestimmte Abnehmer oder Angebotsempfänger in der Aufstellung enthalten sind.
V. Es wird festgestellt, dass, die Beklagten verpflichtet sind, der Klägerin allen Schaden zu ersetzen, der ihr durch die zu I., II. und III. (für Handlungen gemäß III. nur für die Beklagten zu 1) und 3) sowie die Beklagten zu 4) bis 7)) bezeichneten, seit dem 23. September 2006 begangenen Handlungen entstanden ist und noch entstehen wird.
Die Beklagten beantragen:
Die Klage wird abgewiesen.
Die Beklagten behaupten, die Versendung der Blutproben nach Prag zur Durchführung der streitgegenständlichen Untersuchung werde von ihnen nicht angeboten oder beworben.
Die Durchführung des Tests in der Tschechischen Republik hätte den Zweck, den einsendenden Ärzten in Deutschland, wie seit 2005 gewohnt, auch weiterhin eine umfassende Untersuchung der Patientenproben nach einem einheitlichen Standard auf vielerlei Gendefekte zur Verfügung zu stellen. Weiterhin sei für die Erstellung einer Prognose bei einem Patienten mit akuter myeloischer Leukämie (AML) insbesondere die Mutationslast der FLT3-LM von besonderer Bedeutung, welche im Labor der Klägerin bis vor kurzem gar nicht bestimmt worden sei.
Die von ihnen in Deutschland durchgeführten Verfahrensschritte seien für die Durchführung der FLT3-LM Untersuchung nicht notwendig, denn das Nachweisverfahren könne auch mit einer unaufbereiteten Patientenprobe durchgeführt werden.
Die Beklagten meinen, das Vorgehen in Prozessstandschaft sei rechtsmissbräuchlich, weil ihre Prozesskosten in Falle des Obsiegens nicht gedeckt seien. In Anspruch 1 des Streitpatents werde nur eine definitive Feststellung einer Tandemverdopplungsmutation beansprucht. Die Feststellung einer Längenmutation, wie von den Beklagten praktiziert, falle hierunter nicht.
Hinsichtlich der weiteren Einzelheiten wird auf die gewechselten Schriftsätze nebst Anlagen und das Protokoll der mündlichen Verhandlung vom 06.11.2014 Bezug genommen.
Entscheidungsgründe
A.
Die Klage ist zulässig, und zwar auch soweit die Klägerin aus fremdem Recht vorgeht – also in Bezug auf die Unterlassungsansprüche (vgl. S. 3 der Replik). Die Voraussetzungen der gewillkürten Prozessstandschaft sind gegeben. Insbesondere hat die Klägerin ein eigenes rechtsschutzwürdiges Interesse an der Verfolgung des Unterlassungsanspruchs, denn ihr Geschäftsbetrieb ist u. a. darauf ausgerichtet, das streitgegenständliche Verfahren auf dem Markt anzubieten. Rechtsmissbräuchlich wäre die Geltendmachung dieser Rechte durch die Klägerin anstelle ihrer Muttergesellschaft erst, wenn die Klägerin selbst keine realistische Aussicht hätte, von dem wirtschaftlichen Ergebnis des Prozesses zu profitieren (BGH NJW 1999, 1717). So liegt der Fall hier nicht. Vielmehr besteht das Unternehmensziel der Klägerin u. a. gerade darin, Gewinn aus der Durchführung des streitgegenständlichen Verfahrens zu erzielen. Sie hat angesichts der klageseits vorgetragenen Unterstützung durch die Muttergesellschaft – anders als die Klägerin in dem der beklagtenseits zitierten Entscheidung BGH NJW 1986, 850 zugrundeliegenden Sachverhalt – auch realistische Aussichten, dieses Ziel verwirklichen zu können. Diese Unterstützung ist auch glaubhaft und weiterhin in Zukunft zu erwarten. Denn durch die Investition in die Klägerin – etwa in Form von Krediten – hat die Muttergesellschaft der Klägerin die Aussicht, auf dem deutschen Markt Gewinne zu realisieren, sobald der Geschäftsbetrieb der Klägerin im Inland etabliert ist.
B.
Indes ist die Klage unbegründet.
Der Klägerin stehen die geltend gemachten Ansprüche nicht zu.
Gem. Art. 64 EPÜ, §§ 139 Abs.1, 9 S. 2 Nr. 1 und 2 PatG kann von dem Verletzten bei Wiederholungsgefahr auf Unterlassung in Anspruch genommen werden, wer entgegen den §§ 9 bis 13 PatG eine patentierte Erfindung benutzt. Bei Verschulden stehen dem Verletzten auch die hier geltend gemachten Ansprüche auf Auskunft und Schadensersatz zu.
Indes haben die Beklagten nicht eine patentierte Erfindung entgegen den §§ 9 bis 13 PatG benutzt. Daher sind sämtliche geltend gemachten Ansprüche unbegründet. Weder verwenden die Beklagten ein unmittelbares Verfahrenserzeugnis gemäß § 9 S. 2 Nr. 3 PatG in Deutschland, noch liegt eine Patentverletzung unter mittäterschaftlichen Gesichtspunkten gemäß § 9 S. 2 Nr. 2 PatG, noch eine mittelbare Patentverletzung nach § 10 Abs. 1 PatG vor.
I.
Die Kammer hat mangels Aussetzungsantrages der Beklagten vom Rechtsbestand des Anspruchs 7 des Streitpatents auszugehen. Ergänzend wird auf die Ausführungen der Kammer im Urteil vom 25.04.2013 (Az.: 7 O 17048/12), auf die Ausführungen des Bundespatentgerichts in seinem Urteil vom 09.07.2013 (Az.: 3 NI 37/11, hier vorgelegt als Anlage VP 11) sowie weiter ergänzend auf die Ausführungen der Klägerin in der Klageschrift Bezug genommen.
II.
Auch macht das angegriffene Verfahren von Anspruch 1 des Streitpatents (wie aufrechterhalten) wortsinngemäß Gebrauch.
1.
Das Klagepatent betrifft in der aufrechterhaltenen und hier geltend gemachten Form u. a. ein Verfahren zum Nachweis einer Nukleinsäure, die eine Rezeptor-Proteinkinase codiert, welche eine Tandemverdopplung in einer Nukleotidsequenz einer Juxtamembran umfasst.
AML ist eine bösartige Erkrankung des blutbildenden Systems durch abnormale massive Vermehrung unreifer Vorstufen gewisser Zellen im Blut und Knochenmark. Die Bildung reifer Zellen wird dadurch be- bzw. verhindert, was ohne Behandlung zum Tod des Erkrankten führt. Die Zellteilung wird durch Wachstumsfaktoren reguliert. Diese wirken über Rezeptoren. Die Erfindung betrifft solche Rezeptoren, die eine Tyrosinkinase-Domäne enthalten und als Rezeptor-Tyrosinkinasen (RTK) klassifiziert sind. Diese Rezeptoren sitzen in der Membran einer Zelle und besitzen eine extrazelluläre sowie eine intrazelluläre Region. Außerdem besitzen sie eine Transmembran-Region, die innerhalb der Zellmembran liegt, sowie eine Juxtamembran-Region, die nahe der Transmembran-Region im Zellinneren liegt, vgl. die nachfolgende Abbildung:
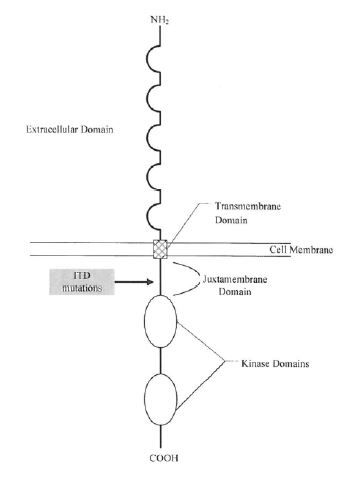
RTK werden durch Liganden aktiviert, beispielsweise durch die vorstehend genannten Wachstumsfaktoren, die an die extrazelluläre Region der RTK binden, was zur Aktivierung der Kinase führt. Die im Klagepatent genannte RTK ist die so genannte fms-ähnliche Tyrosinkinase 3 (FLT3), die bei der Zellteilung von blutbildenden Stammzellen und Leukämie entdeckt worden ist. Die fms-ähnliche Tyrosinkinase 3 (FLT3) war aus einer Reihe von wissenschaftlichen Veröffentlichungen vorbekannt.
Tyrosinkinasen werden in Körperzellen durch Ribosome hergestellt. Die Anleitung zur Herstellung bestimmter Proteine erhalten die Ribosome durch so genannte Messenger-RNA (mRNA), die die genetische Information zur Herstellung der Proteine enthält. Die mRNA, ein einkettiger Nukleinsäurestrang, erhält ihre Information wiederum aus DNA, die sich bei menschlichen Zellen im Zellkern in Form von Chromosomen befindet. Die Information zur Herstellung der abnormalen, eine Tandemverdopplungsmutation aufweisenden FLT3 liegt damit bereits im Code der chromosomalen DNA vor und wird dann über die mRNA in das Protein weitergegeben.
2.
Der zuständige Fachmann ist vorliegend als Team zu definieren, das aus einem Molekularbiologen mit praktischer Erfahrung in der Tumorbiologie sowie einem Mediziner mit Erfahrung in der Behandlung hämatologischer Erkrankungen besteht (vgl. S. 23 des als Anlage VP 11 vorgelegten Urteils des BPatG vom 09.07.2013).
3.
Zum Stand der Technik gehören Untersuchungsverfahren, mittels derer die Aminosäuresequenz des FLT3-Proteins bestimmt wurden, ohne dass Struktur und Funktion von FLT während der Differenzierung der blutbildenden Stammzellen und die bösartigen Veränderungen an leukämischen Zellen näher untersucht worden wären (vgl. Abschnitt [0011] des Klagepatents).
4.
Das Klagepatent kritisiert am Stand der Technik, dass die Struktur und Funktion von FTL während der Differenzierung der blutbildenden Stammzellen und die bösartigen Veränderungen an leukämischen Zellen bisher nicht gut genug untersucht worden seien.
5.
Es stellt sich vor diesem Hintergrund die Aufgaben, eine Nucleinsäure bereitzustellen, die eine Rezeptor-Proteinkinase codiert, wobei die Nucleinsäure eine Tandemverdoppelung in einer Nucleotidsequenz einer Juxtamembran besitzt und für die Diagnose von Leukämie von Nutzen ist (Abschnitt 12).
6.
Aus dem Vorhandensein der in Anspruch 1 beschriebenen Nukleinsäure, beispielsweise in der Serumprobe eines Menschen, kann nach Auffassung des Klagepatents eine Prognose hinsichtlich des schlechten Verlaufs einer akuten myeloischen Leukämie (AML) gestellt werden, so dass die Präsenz der Nukleinsäure in der Prognostik dieser Krankheit eine große Rolle spielt.
Biotechnologisch kann man sich diesen vom Klagepatent beschriebenen Ablauf zu Nutzen machen, indem man denjenigen Abschnitt der DNA, der das betreffende Protein kodiert, bzw. einen noch kleineren Abschnitt davon, der nur bestimmte Bereiche des Proteins kodiert, wie beispielsweise vorliegend den mutierten Bereich der Juxtamembran von FLT3, selektiert, mithilfe bekannter Verfahren wie beispielsweise der Polymerase-Kettenreaktion (PCR) zur Überprüfung der DNA oder einer Überprüfung der RNA unter Verwendung der reversen Transkriptase-Polymerase-Kettenreaktion (RT-PCR) massenhaft amplifiziert und dann untersucht, ob sich in diesem Bereich eine Längenmutation befindet. Dies ermöglicht es dem Arzt, allein dadurch einem Patienten eine entsprechende Diagnose zu stellen, dass er eine Serumprobe des Patienten an ein Diagnoselabor übergibt. Dieses selektiert dann auf bekannte Art und Weise den Abschnitt der DNA, der die Juxtamembran von FLT3 kodiert. Diesen Bereich amplifiziert das Labor mithilfe der PCR oder RT-PCR und untersucht dann, wieder mithilfe bekannter Diagnoseverfahren wie beispielsweise der Agarose-Gelelektrophorese, der Kapillarelektrophorese oder der Sequenzierung, ob eine Genmutation vorhanden ist oder nicht. In der mutierten Gensequenz findet sich, wie nachfolgend dargestellt, die mit „ITD“ bezeichnete Längenmutation (rechte Gensequenz), während sich im Wildtyp-Allel diese Mutation nicht findet (linke Gensequenz):
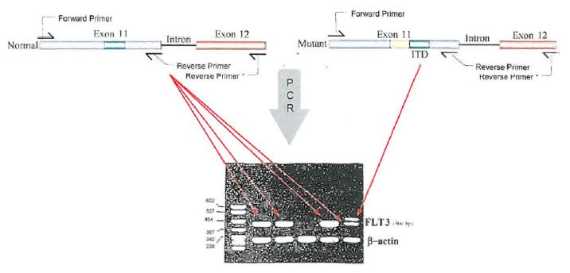
Bei der RT-PCR wird nun der Teil des Gens, der von Interesse ist, weil er die mögliche Mutation beinhaltet, mithilfe eines Primerpaars (forward und reverse primer) amplifiziert. Nach der Amplifizierung des Ausschnitts der Gensequenz wird, wie vorstehend in der Graphik anhand einer Agarose-Gelelektrophorese gezeigt, analysiert, ob eine Mutation vorhanden ist. Die linke Gelspur zeigt einen aufgetrennten Längenmarker, der Fragmente bekannter Länge enthält (siehe angegebene Fragmentlängen in Basenpaaren). Die längeren Sequenzen bewegen sich aufgrund ihrer Größe im Gel (von oben nach unten gesehen) über denselben Zeitraum betrachtet langsamer und befinden sich daher in der Abbildung weiter oben als die kürzeren. Anhand dieser Referenz-DNA-Fragmente, deren Länge bekannt ist, kann man die Länge eines FLT3 DNA-Ausschnitts bestimmen, weil Fragmente gleicher Länge die gleiche Strecke im Gel zurücklegen. Neben der Amplifizierung der Ziel-DNA wird meist ebenfalls ein interner Standard mitamplifiziert, um zu überprüfen, ob die PCR funktioniert hat. In dem der Abbildung zugrunde liegendem Experiment wurde ?-actin, zu sehen in der unteren rechten Zeile, als interner Standard verwendet. Anhand der in allen Gelspuren sichtbaren ?-actin-Bande können folgende Rückschlüsse gezogen werden: 1. die PCR sollte bei allen zu analysierenden Proben funktioniert haben (wäre dies nicht der Fall, würde keine ?-actin-Bande zu sehen sein, weil keine Amplifikation stattgefunden hat), und 2. die Menge an auf das Gel aufgetragener Probe ist ungefähr gleich für alle Proben, weil die Bandendicke ungefähr gleich ist, so dass ausgeschlossen werden kann, dass ein negatives Ergebnis durch das Auftragen von zu wenig amplifiziertem Probenmaterial verursacht wurde. Durch diese Kontrolle wird die analytische Qualität des Verfahrens erhöht. In der rechten oberen Zeile finden sich die Ergebnisse der verschiedenen Proben in Hinblick auf die zu untersuchende Gensequenz. Man kann erkennen, dass bei den ersten drei Proben von links gesehen keine Mutation vorhanden ist, denn die Amplifikate dieser drei Proben sind alle im Gel gleich weit migriert; sie besitzen also alle dieselbe Länge. Die rechte Probe weist Amplifikate mit zwei unterschiedlichen Längen auf: eine Bande ist genauso weit migriert wie die Amplifikate der vorhergenannten drei Proben, sie besitzen also dieselbe Länge; die zweite Bande liegt über der ersten Bande und das diese Bande bildende Amplifikat besitzt deswegen eine längere Sequenz. Diese Zunahme der Amplifikatlänge trotz der Verwendung gleicher Primer korreliert mit dem Vorkommen von Längenmutationen, die innerhalb des amplifizierten Genabschnitts auftreten. Die Tatsache, dass zwei Banden im Gel sichtbar sind, lässt sich durch das zweimalige Vorkommen des FLT3-Gens pro Zelle erklären (Diploidie). In diesem Fall besitzt der Mensch, dem die Probe entnommen wurde, eine nicht-mutierte FLT3-Genkopie und eine mutierte FLT3-Genkopie. Dementsprechend gibt es auch den Fall, dass beide FLT3-Genkopien Längenmutationen tragen. Dann wäre, sofern beide FLT3-Genkopien dieselbe Längenmutation tragen, nur eine Bande zu erkennen, die sich im Vergleich zu einer nicht-längenmutierten Sequenz, also der Wildtypsequenz, allerdings weiter oben im Gel befände.
7.
Zu Gegenstand des Anspruchs 1:
a.
Die Kammer legt ihrer Auslegung folgende Merkmalsgliederung von Anspruch 1 zugrunde:
Verfahren zum Nachweis eines Nukleinsäuremoleküls einer Tandemverdopplungsmutante, das humane FMS-artige Tyrosinkinase 3 (FLT3) codiert, wobei das Nukleinsäuremolekül eine Nucleotidsequenz hat entsprechend: einer Tandemverdopplungsmutation in der Nucleotidsequenz [einer Region umfassend] von Exon 11 oder Exons 11 bis 12 von FLT3 ohne Verschiebung des Leserasters, die durch Primer der SEQ ID No. 26 und SEQ ID NO: 27 amplifiziert werden kann und als Längenmutation nachweisbar ist, umfassend die Schritte:
a)
Durchführung einer Genamplifikationsreaktion mit einer Nukleinsäureprobe von einem Menschen, wobei ein Nukleinsäurefragment, das Exon 11 oder Exons 11 bis 12 des FMS-artigen Tyrosinkinase 3 (FLT3)-Gens umfasst und eine Tandemverdopplungsmutation in der Juxtamembran hat, amplifiziert wird, welches im FLT3-Gen gefunden werden kann;
b)
Nachweis der Anwesenheit der Tandemverdopplungsmutation in dem Nukleinsäurefragment aus Schritt a).
Dabei hat die Kammer berücksichtigt, dass die englischsprachige Version verbindlich ist, sie hält allerdings – wie auch die Parteien – die vorgelegte Übersetzung für zutreffend.
b.
In Schritt (2) (a) wird die Durchführung einer Genamplifikationsreaktion eines Nukleinsäurefragments beansprucht. Die Herstellung des Nukleinsäurefragments ist hingegen nicht Teil des beanspruchten Verfahrens. Die hierfür erforderliche Isolation der DNA ist daher vielmehr nur eine (nach Kenntnis des Fachmanns) erforderliche Vorbereitungshandlung zur Durchführung des beanspruchten Verfahrens.
c.
Anspruch 1 erfordert in Schritt (2) (b) nicht einen über den Längenvergleich hinausgehenden Nachweis einer Tandemverdopplungsmutation – etwa in Form der Sequenzierung der DNA. Insoweit wird primär auf das Urteil der Kammer vom 25.04.2013, Az. 7 O 17048/12) verwiesen.
Zusammenfassend wird angemerkt: Zwar trifft es zu, dass in Anspruch 1 (2) (b) wörtlich ausgeführt wird, eine Tandemverdopplungsmutation sei nachzuweisen („detecting“). Insoweit gilt aber, dass nach Art. 69 Abs. 1 EPÜ der Schutzbereich des Patents durch den Inhalt der Patentansprüche bestimmt wird, wobei die Beschreibung und die Zeichnungen zur Auslegung der Patentansprüche heranzuziehen sind. Inhalt bedeutet nicht Wortlaut, sondern Sinngehalt. Maßgebend ist der Offenbarungsgehalt der Patentansprüche und ergänzend – im Sinne einer Auslegungshilfe – der Offenbarungsgehalt der Patentschrift, soweit dieser Niederschlag in den Ansprüchen gefunden hat. Entscheidend für die Beurteilung ist die Sicht des in dem jeweiligen Fachgebiet tätigen Fachmanns. Begriffe in den Patentansprüchen und in der Patentbeschreibung sind so zu deuten, wie sie der angesprochene Durchschnittsfachmann nach dem Gesamtinhalt der Patentschrift unter Berücksichtigung von Aufgabe und Lösung der Erfindung versteht. Bei der Auslegung ist nicht am Wortlaut zu haften, sondern es ist auf den technischen Gesamtzusammenhang abzustellen, den der Inhalt der Patentschrift dem Durchschnittsfachmann vermittelt. Der Patentanspruch ist nicht wörtlich in philologischer Betrachtung, sondern seinem technischen Sinn nach aufzufassen. Der Erfindungsgedanke muss unter Ermittlung von Aufgabe und Lösung bestimmt werden, wie sie sich aus dem Patent ergeben. Bei der Feststellung, welchen Sinngehalt der Durchschnittsfachmann den Merkmalen des Patentanspruchs entnimmt, ist stets der Gesamtzusammenhang des Patentanspruchs im Auge zu behalten. Feststellungen zum Inhalt einzelner Merkmale dienen nur dazu, schrittweise den allein maßgeblichen Wortsinn des Patentanspruchs als Einheit zu ermitteln (vgl. BGH GRUR 2004, 845 ff. – Drehzahlermittler).
Hiervon ausgehend und angesichts der Systematik der Ansprüche 1 – 4 sowie der Erläuterungen in der Patentschrift ist der Begriff „detection“ in Anspruch 1 (2) (b) so zu interpretieren, dass der anspruchsgemäße „Nachweis“ einer Tandemverdopplungsmutation bereits durch die Feststellung einer Längenmutation erbracht ist.
aa.
Hierfür spricht bereits die Systematik der Patentansprüche 1 – 4, die von einer allgemeinen Beschreibung hin zum Schutz eines speziellen Verfahrens führt: In Anspruch 1 (2) (b) wird nur allgemein von einem Nachweis einer Tandemverdopplungsmutation gesprochen, ohne dass mitgeteilt wird, auf welche Weise dieser Nachweis geführt werden soll. Etwas konkreter ist Anspruch 3 gefasst, in welchem vorgesehen ist, dass der Nachweis einer Tandemverdopplungsmutation durch Vergleich des amplifizierten Nukleinsäurefragments mit einer normalen Sequenz erfolgt. In Anspruch 4 wird schließlich beansprucht, dass in Schritt (2) (b) des Anspruchs 1 eine Längenmutation als Index für die Tandemverdopplungsmutation verwendet wird. Dabei ist Anspruch 3 noch etwas allgemeiner gehalten, als Anspruch 4, denn in Anspruch 3 wird noch nicht beschrieben, was genau verglichen werden soll. Dass (nur) die Längen der amplifizierten Segmente zu vergleichen sind, wird erst in Anspruch 4 beschrieben.
bb.
Auch die Beschreibung gibt deutlich zu erkennen, dass nach der Diktion der Patentschrift von einem Nachweis einer Tandemverdopplungsmutante bereits dann ausgegangen werden kann, wenn eine Längenmutation im beanspruchten Bereich festgestellt werden kann. Insoweit wird insbesondere auf Abschnitt [0044] verwiesen. Dort wird ausgeführt, dass der Längenvergleich eine mögliche – ja vorzugswürdige – Methode des Nachweises einer Tandemverdopplungsmutation sein könne. Hierdurch wird klar, dass der Erfinder den Längenvergleich gerade nicht als Zwischenschritt vor Durchführung des eigentlichen Nachweisverfahrens vorschlägt, sondern dass er in dem Längenvergleich selbst ein vollwertiges Nachweisverfahren sieht.
cc.
Dieses Auslegungsergebnis deckt sich im Übrigen mit der Auslegung des Bundespatentgerichts (vgl. das als Anlage VP 11 vorgelegte Urteil vom 09.07.2013, S. 30 f.).
III.
Indes verwenden die Beklagten weder ein unmittelbares Verfahrenserzeugnis gemäß § 9 S. 2 Nr. 3 PatG in Deutschland, noch liegt eine Patentverletzung unter mittäterschaftlichen Gesichtspunkten gemäß § 9 S. 2 Nr. 2 PatG, noch eine mittelbare Patentverletzung nach § 10 Abs. 1 PatG vor.
1.
Nach Art. 64 EPÜ, §§ 139 Abs.1, 9 S. 2 Nr. 3 PatG kann die Klägerin zwar von den Beklagten verlangen, es zu unterlassen, das durch ein Verfahren, das Gegenstand des Patents ist, unmittelbar hergestellte Erzeugnis anzubieten, in Verkehr zu bringen oder zu gebrauchen oder zu den genannten Zwecken entweder einzuführen oder zu besitzen. Indes handelt es sich bei der durch das streitgegenständliche Verfahren gewonnenen Information nicht um ein unmittelbar hergestelltes Erzeugnis.
a.
Da die Verletzung eines Europäischen Patents gem. Art. 64 Abs. 3 EPÜ nach nationalem Recht zu behandeln ist, ist für die Auslegung die deutsche Fassung des Art. 64 Abs. 2 EPÜ heranzuziehen. Die nachfolgend erläuterte Interpretation der Kammer trifft allerdings gleichermaßen auch auf die englische („products directly obtained by such process“) und die französische Fassung („produits obtenus directement par ce procédé“) zu (vgl. Art. 177 Abs. 1 EPÜ), deren Übereinstimmung mit der deutschen Fassung ohnehin vermutet wird (Benkard/Schäfers 2. Aufl Art. 177 EPÜ Rn. 4).
aa.
Das Erfordernis der „Unmittelbarkeit“ bedeutet, dass das gewonnene Erzeugnis in der ins Inland gelangten Form Ergebnis des geschützten Verfahrens sein muss und mit Abschluss seines letzten Schritts erhalten wird (Mes, 3. Aufl., § 9 PatG Rn. 64 mwN.). Irrelevant ist hingegen, in welcher Weise oder auf welchem (Daten-)Träger es dorthin verbracht wird (BGH GRUR 2012, 1230, 1233 – MPEG-2-Videosignalcodierung).
Diese Voraussetzung ist vorliegend gegeben, denn die infolge des Diagnoseverfahrens erhaltene Information wird unverändert nach Deutschland übermittelt. Die Verkörperung der gewonnenen Erkenntnis auf einem Schrift- oder Datenträger steht dem Unmittelbarkeitserfordernis nicht entgegen (BGH GRUR 2012, 1230, 1233 – MPEG-2-Videosignalcodierung).
bb.
Durch ein Verfahren „hergestellt“ ist ein Erzeugnis jedenfalls immer dann, wenn es durch ein Herstellungsverfahren hervorgebracht worden ist. Das setzt voraus, dass ein Endprodukt hergestellt wird, welches von einem etwaigen Ausgangsprodukt abweicht. Während das bei handwerklichen wesentlichen Veränderungen von Gegenständen stets zu bejahen ist, stellen Reinigung, Prüfung und Reparatur keine Herstellungs-, sondern Arbeitsverfahren dar (Mes, 3. Aufl., § 9 PatG Rn. 63; ders. GRUR 2009, 305, 307 f. jew. mwN.; vgl. auch RG GRUR 1939, 477, 480 – Prüfung eines Hochvakuumgefäßes auf Dichtigkeit).
Angesichts dessen ist die gewonnene, streitgegenständliche Information Ergebnis eines Herstellungsverfahrens. Zwar wird bei der Untersuchung der Blutprobe lediglich eine Veränderung derselben vorgenommen. Käme es auf die Blutprobe an, würde es sich um ein Arbeitsverfahren handeln. Indes dient das Verfahren ausweislich der Patentansprüche nicht der Gewinnung einer Blutprobe mit bestimmten Eigenschaften, sondern dem Nachweis eines Nukleinsäuremoleküls. Diese gewonnene Information war indes zuvor für die menschliche Erkenntnis so nicht verfügbar, so dass in Bezug auf sie von einem Herstellungsverfahren auszugehen ist (so für Gentests bereits OLG Düsseldorf InstGE 12, 258 ff. – Blut/Gehirnschranke).
cc.
Die streitgegenständliche Erkenntnis ist jedoch kein „Erzeugnis“.
(1)
Auch unkörperliche Gegenstände können derivativen Erzeugnisschutz im Sinne des § 9 Satz 2 Nr. 3 PatG beanspruchen. Voraussetzungen hierfür sind, dass der unkörperliche Gegenstand in gleichem Maße wie ein körperlicher Gegenstand handelbar sowie mit Hilfe von Speicher- und ggf. auch Wiedergabemedien immer wieder benutzbar ist wie ein durch das geschützte Verfahren hervorgebrachter körperlicher Gegenstand; darüber hinaus muss er aufgrund seiner Handel- und Wiederbenutzbarkeit einen Marktwert besitzen, der sich nicht durch eine einmalige Informationsübermittlung erschöpft. Ferner muss der unkörperliche Gegenstand noch eine Prägung durch die erfindungswesentlichen Merkmale des geschützten Verfahrens aufweisen (Fortführung von BGH GRUR 2012, 1230 – MPEG-2-Videosignalcodierung).
Der Anwendungsbereich des § 9 S. 2 Nr. 3 PatG erstreckt sich hingegen nicht auf durch ein Verfahren hervorgebrachte Informationen, die bereits durch das menschliche Gedächtnis unkompliziert speicherbar sind und verbal kommuniziert werden können und deren wirtschaftlicher Wert sich durch die einmalige Informationsübermittlung erschöpft (Bestätigung von OLG Düsseldorf InstGE 12, 258 ff. – Blut/Gehirnschranke).
Im Einzelnen:
(a)
Hintergrund des derivativen Erzeugnisschutzes nach § 9 S. 2 Nr. 3 PatG ist die Vorstellung, dass der Inhaber eines Verfahrenspatents den ihm zustehenden wirtschaftlichen Wert der Erfindung nicht in angemessener Weise ausschöpfen könne, wenn ihm nicht neben der Anwendung des Verfahrens auch der Handel mit den dadurch hergestellten Erzeugnissen vorbehalten ist (Mes, GRUR 2009, 305 mwN.). Durch diese Regelung soll sichergestellt werden, dass der Inhaber des Verfahrenspatents den wirtschaftlichen Wert der Erfindung in angemessener Weise nicht nur durch die Anwendung des Verfahrens sondern auch den Handel mit den dadurch unmittelbar hergestellten Erzeugnissen ausschöpfen kann (Haedicke/Timmann, Handbuch des Patentrechts § 8 Rn. 57). Der Erzeugnisschutz findet sich inhaltsgleich in Art. 64 Abs. 2 EPÜ und Art. 28 Abs. 1 TRIPS.
(b)
Die Regelung wurde in das deutsche Patentgesetz im Jahr 1891 aufgenommen, weil damals kein Patentschutz für chemische Stoffe bestand (Cimniak: Der derivative Erzeugnisschutz im deutschen Patentrecht, Münster 2014 S. 43 – 48; Fitzner/Lutz/Bodewig/Ernsthaler, Patentrechtskommentar 4. Aufl. § 9 Rn. 54).
Der damals formulierte § 4 PatG lautete: „Das Patent hat die Wirkung, daß der Patentinhaber ausschließlich befugt ist, gewerbsmäßig den Gegenstand der Erfindung herzustellen, in Verkehr zu bringen, feilzuhalten oder zu gebrauchen. Ist das Patent für ein Verfahren ertheilt, so erstreckt sich die Wirkung auch auf die durch das Verfahren unmittelbar hergestellten Erzeugnisse.“
§ 4 des Patentgesetzes von 1877 lautete noch: „Das Patent hat die Wirkung, daß niemand befugt ist, ohne Erlaubniß des Patentinhabers den Gegenstand der Erfindung gewerbsmäßig herzustellen, in Verkehr zu bringen oder feilzuhalten. Bildet ein Verfahren, eine Maschine oder eine sonstige Betriebsvorrichtung, ein Werkzeug oder ein sonstiges Arbeitsgeräth den Gegenstand der Erfindung, so hat das Patent außerdem die Wirkung, daß niemand befugt ist, ohne Erlaubniß des Patentinhabers das Verfahren anzuwenden oder den Gegenstand der Erfindung zu gebrauchen.“
(c)
Es besteht kein Zweifel, dass körperliche Gegenstände Erzeugnisse sein können (Mes, 3. Aufl., § 9 PatG Rn. 62 und ders. GRUR 2009, 305 jew. mwN.).
(d)
Auch ist es richtig, den Sachschutz auf unkörperliche Signalfolgen zu erstrecken, die mittels elektronischer Speicher-, Übermittlungs- und Wiedergabemedien archiviert, übertragen und – immer wieder – genutzt werden können, denn derartige Codierungen sind wie körperliche Gegenstände handelbar, besitzen also einen Marktwert, der sich nicht durch eine einmalige Informationsübermittlung erschöpft und auf Null reduziert (BGH GRUR 2012, 1230, 1233 f. – MPEG-2-Videosignalcodierung). Dieses Verständnis ist auch noch mit dem Wortlaut des § 9 S. 2 Nr. 3 PatG vereinbar, denn derartige Signalfolgen können ohne eine Verkörperlichung auf Datenträgern nicht aufbewahrt und erst recht nicht gehandelt werden. Auch nach einer Übertragung über das Internet befinden sie sich wieder auf einem Datenträger – und sei es nur im flüchtigen Cache eines Computers.
(e)
Es verbietet sich hingegen, den Anwendungsbereich des § 9 S. 2 Nr. 3 PatG auf Informationen zu erstrecken, die bereits durch das menschliche Gedächtnis unkompliziert speicherbar sind (vgl. i. E. auch OLG Düsseldorf InstGE 12, 258 ff. – Blut/Gehirnschranke).
(aa)
Vor dem Hintergrund, dass die Art. 64 APÜ, §§ 139, 9 PatG Eingriffsnormen sind, ist Zurückhaltung gegenüber einer zu extensiven Anwendung dieser Vorschriften geboten.
Es gilt zwar nicht das strenge Bestimmtheitserfordernis wie im Strafrecht, gleichwohl sind einer Überdehnung des Wortlauts insbesondere vor dem Hintergrund der Nachahmungsfreiheit Grenzen gesetzt. Der vom Verb „Zeugen“ abstammende Begriff des Erzeugnisses enthält ethymologisch durchaus eine körperliche Komponente. Er ist insbesondere von dem Begriff der Erkenntnis abzugrenzen.
(bb)
Aus derselben Erwägung heraus wird von der absolut überwiegenden Auffassung zutreffend der Erzeugnisschutz nach § 9 S. 2 Nr. 3 PatG für unkörperliche Verfahrensergebnisse wie Licht, Wärme, elektrische Energie oder Schall durchweg abgelehnt (vgl. Benkard/Scharen 10. Aufl. § 9 PatG Rn. 53; Busse/Keukenschrijver 6. Aufl. § 9 PatG Rn. 100).
(cc)
Nicht überzeugend ist die Auffassung der Klägerin, die ratio legis greife bei Verfahren wie dem streitgegenständlichen voll durch, weil die gegenwärtige Situation vergleichbar sei mit der Situation Ende des 19. Jahrhunderts, als es noch einen Patentierungsausschluss für chemische Stoffe gab; gerade dieser Ausschluss habe damals überhaupt erst zur Implementierung des derivativen Erzeugnisschutzes in das deutsche Patentgesetz von 1891 geführt. Anders als bei chemischen Stoffen – und auch Videosignalfolgen – ist die Handelbarkeit der durch das streitgegenständliche Verfahren gewonnenen Information nicht uneingeschränkt gegeben, insbesondere lässt sie sich nicht beliebig oft weiter geben. Vielmehr ist nach einmaliger Mitteilung der Erkenntnis ob oder ob nicht die Genmutation in dem Nucleinsäurefragment nachgewiesen werden konnte, an den Patienten bzw. seinem Arzt der wirtschaftliche Wert des Verfahrens verbraucht. Im Übrigen ließe sich eine Anwendung des § 9 S. 2 Nr. 3 PatG über den Wortlaut hinaus nicht mit dem Argument rechtfertigen, dass dies rechtspolitisch wünschenswert sei. Vielmehr ist gerade im Bereich von Eingriffsnormen die Fortentwicklung des Rechts vornehmliche Aufgabe des Gesetzgebers. Das nicht in Kraft getretene Gemeinschaftspatentübereinkommen (vgl. die Ausführungen der Klägerin auf S. 9 ihrer Replik) liefert gleichfalls keinen Anhalt zur Interpretation der bestehenden Gesetzeslage.
Die Klägerin argumentiert weiter, das Dilemma des Patentinhabers liege bei Diagnoseverfahren insoweit darin, dass er nur aufgrund von generellen, für die vorliegenden Verfahren nicht einmal besonders hinterfragten Patentierungsausschlüssen einen Verfahrensschutz wählen müsse, während im Grunde ein Erzeugnisschutz angebracht sei; rechtspolitisch sei ein Erzeugnisschutz für durch Diagnoseverfahren gewonnene Verfahrensergebnisse wünschenswert, handele es sich doch bei diesen Verfahren oft um wichtige Verfahren für die Volksgesundheit; wolle man entsprechende Innovation auf diesem wichtigen technischen Gebiet fördern, müsse der Schutz des geistigen Eigentums entsprechend wirkungsvoll gestaltet sein. Gerade dieser Gedanke spricht allerdings in besonderem Maße dafür, der gewonnenen Information den Erzeugnisschutz de lege lata zu versagen. Denn nachdem der Gesetzgeber bewusst Patentierungsausschlüsse im Bereich medizinischer Verfahren vorgenommen hat, darf von der Rechtsprechung dieses gesetzgeberische Ziel nicht durch eine extensive Anwendung des Erzeugnisschutzes umgangen werden. Wenn tatsächlich die gegenwärtige Situation mit dem Patentierungsausschluss für chemische Stoffe vergleichbar sein sollte, wäre der Gesetzgeber wie schon im Jahr 1891 zum Handeln aufgefordert. Die Rechtsprechung hat die gesetzgeberische Entscheidung zu achten, nach der bloße Informationen gem. §§ 1 S. 2 Nr. 4, 9 S. 2 Nr. 3 PatG keinen Patentschutz genießen (vgl. auch Mes GRUR 2009, 305, 306).
(dd)
Die Einfachheit des Untersuchungsergebnisses ist durchaus ein relevanter Faktor bei der Subsumtion unter den Erzeugnisbegriff. Denn wenn Daten nur in verkörperter Form praktisch verwendet werden können, stehen sie wirtschaftlich einem körperlichen Gegenstand gleich. Wenn eine Information (vorliegend: eine Längenmutation wurde gefunden oder nicht gefunden) anders als bei einer Videosignalcodierung aber rein intellektuell festgehalten und verbal kommuniziert werden kann, bedarf es gerade nicht ihrer Verkörperung, um ihren wirtschaftlichen Wert nutzen zu können.
(f)
Schließlich ist jedenfalls bei unkörperlichen Gegenständen zu fordern, dass der Gegenstand, der derivativen Erzeugnisschutz genießen soll, noch eine Prägung durch die erfindungswesentlichen Merkmale des geschützten Verfahrens aufweist, was naturgemäß meist nur bei einem Herstellungsverfahren bejaht werden kann. Denn bei Sachverhalten mit Auslandsbezug bedarf es eines greifbaren Kriteriums, mit Hilfe dessen ein dem Erzeugnisschutz zugänglicher Gegenstand definiert werden kann. Das Unmittelbarkeitserfordernis bei Verfahrenserzeugnissen bringt es mit sich, dass dem Erzeugnis die Herkunft aus einem patentrechtlich geschützten Verfahren in nachprüfbarer Weise anhaften muss. So ist beispielsweise bei der MPEG-2-Videosignalcodierung das Erzeugnis – also die kodierten Videodaten als Gesamtheit – von dem erfindungsgemäßen Kodierverfahren geprägt. In diese Richtung geht sogar das Verständnis der Klägerin, die auf S. 2 unten der Triplik vom 29.10.2014 ausführt, dass ein Verfahrenserzeugnis die technische Qualität des ihm zugrundeliegenden Verfahrens wiederspiegele.
(2)
Die vorgenannten Voraussetzungen sind bei der streitgegenständlichen Übermittlung der Information über das Untersuchungsergebnis jedoch nicht gegeben.
(a)
Das Untersuchungsergebnis ist eine unverkörperte Information. Der vorliegende Fall ist auch nicht mit der Übermittlung von Datenfolgen wie bei einer Videosignalcodierung (vgl. BGH GRUR 2012, 1230, 1233 – MPEG-2-Videosignalcodierung) vergleichbar. Gegenstand des Streitpatents ist ein Verfahren, welches eine einfache Information ergibt. Die Information kann nur „Ja“ oder „Nein“ bzw. „0″ oder „1″ bzw. „Tandemverdopplungsmutation vorhanden“ oder „nicht vorhanden“ lauten. Zwar untersuchen die Beklagten nicht nur ein einzelnes FLT3-Gen auf eine Tandemverdopplungsmutation, sondern bestimmen die Mutationslast, welche in Form eines Bruchteils bzw. Prozentsatzes übermittelt wird. Diese Information ist aber nicht Ergebnis einer einmaligen, sondern einer vielfachen Anwendung des streitgegenständlichen Verfahrens, könnte mithin schon von vorneherein nicht „das … Erzeugnis“ iSd. § 9 S. 2 Nr. 3 PatG, sondern nur eine Vielzahl derartiger Erzeugnisse sein. Anders, als die Klägerin auf S. 10 der Replik suggeriert, geht es im vorliegenden Fall daher in der Tat um die Frage, ob eine einfache Information unter den Erzeugnisbegriff subsumiert werden kann. Wie ausgeführt, ist die Einfachheit des Untersuchungsergebnisses durchaus ein relevanter Faktor bei der Subsumtion unter den Erzeugnisbegriff. Denn anders als bei einer Videosignalcodierung kann im vorliegenden Fall das Untersuchungsergebnis schon rein intellektuell festgehalten und rein verbal kommuniziert werden. Es bedarf hier gerade nicht einer Verkörperung der Information, um ihren wirtschaftlichen Wert nutzen zu können. Bei dem streitigen Untersuchungsergebnis handelt es sich letztlich nur um eine Erkenntnis und kein Erzeugnis. Diese Begriffe sind – wie gezeigt – voneinander abzugrenzen. Die Beklagten nehmen innerhalb des fraglichen Genabschnitts, welcher vervielfältigt wird, gerade keine Veränderung an der molekulargenetischen Substanz vor – etwa indem sie den genetischen Code verändern; vielmehr vervielfältigen (amplifizieren) sie einen Ausschnitt des Gens und lesen die Länge dieses Abschnitts nur aus. Zur Durchführung des Verfahrens werden zwar in der Natur nicht vorkommende Amplifikate erzeugt. Diese stellen jedoch nicht das patentgemäße Verfahrensergebnis dar, denn sie weisen – für sich genommen – nicht den zu erbringenden Nachweis des Vorliegens einer Tandemverdopplungsmutation oder einer Längenmutation auf, denn es fehlt noch der wertende Vergleich mit einer gesunden Probe. Wenn aber schon das körperliche Produkt des geschützten Verfahrens – nämlich der amplifizierte Genabschnitt – patentfrei ist, kann durch Einführung einer bloßen Beschreibung dieses Produkts erst recht nicht in den ausschließlichen Zuweisungsgehalt des Patents eingegriffen werden.
(b)
Auch weist die streitgegenständliche Information nicht die Prägung durch die erfindungswesentlichen Merkmale des geschützten Verfahrens auf. Vielmehr lässt sich der Aussage, eine Tandemverdopplungsmutation liege vor oder liege nicht vor, mitnichten entnehmen, woher diese Erkenntnis stammt. Im Stand der Technik war bereits bekannt, zur Prognose des Verlaufs einer AML nach einer Tandemverdopplungsmutation zu suchen, etwa durch Sequenzierung des DNA. Gegenstand der Erfindung ist v. a. ein Verfahren zur Ermittlung einer Längenmutation, deren Vorliegen den Schluss auf eine Tandemverdopplungsmutation ermöglichen soll. Dem Endergebnis kann man somit nicht ansehen, durch welches Verfahren es gefunden worden oder ob überhaupt eine Untersuchung vorgenommen worden ist. Mithin ist das Ergebnis bzw. der Gegenstand, der derivativen Erzeugnisschutz genießen soll, anders als beispielsweise bei der MPEG-2-Videosignalcodierung (vgl. hierzu oben Punkt 1. a. cc. (6)) nicht von den erfindungswesentlichen Merkmalen geprägt. Auch die Klägerin zeigt nicht auf, in welcher Weise diese Information ihrer Meinung nach „die technische Qualität des“ ihr „zugrundeliegenden Verfahrens“ wiederspiegele.
(c)
Schließlich ist die Erkenntnis, ob eine Tandemverdopplungsmutation vorliegt oder nicht, nicht wie ein körperlicher Gegenstand handelbar und immer wieder benutzbar. Vielmehr erschöpft sich ihr Nutzen mit ihrer einmaligen Erlangung. Hingegen sind beispielsweise codierte Videodaten nicht nur einmal als Information vollständig für immer durch den menschlichen Geist aufnehmbar, sondern müssen immer wieder vom Nutzer mittels entsprechender Geräte abgespielt werden, um mit ihrem vollen Informationsgehalt und Unterhaltungswert Präsenz im menschlichen Bewusstsein zu genießen.
2.
Auch liegt keine Patentverletzung unter mittäterschaftlichen Gesichtspunkten gemäß § 9 S. 2 Nr. 2 PatG vor.
Die Verantwortlichkeit für eine Patentverletzung setzt zwar nicht voraus, dass der Inanspruchgenommene selbst in eigener Person eine der in § 9 Satz 2 PatG bezeichneten Handlungen vornimmt (BGH GRUR 2009, 1142 – MP3-Player-Import). Eine mittäterschaftliche Verletzung setzt allerdings eine wesentliche, die Täterschaft, also Tatherrschaft begründende Mitwirkungshandlung im Inland voraus. Erforderlich wäre, dass einer der Antragsgegner eine inländische Patentverletzung bewusst und willentlich mitverursacht hat (GRUR 2002, 599 – Funkuhr). Denn Mittäterschaft und Beihilfe setzen ein bewusstes und gewolltes Zusammenwirken bei Benutzungshandlungen im Sinne von §§ 9, 10 PatG voraus (Mes, 3. Aufl., § 9 PatG Rn. 114). Insbesondere die Durchführung im Anspruch genannter Verfahrensschritte im Inland kann eine mittäterschaftliche Zurechnung im Ausland vollzogener Verfahrensschritte bewirken (OLG Düsseldorf Mitt. 2010, 237 ff. – Prepaid-Telefonkarte).
Vorliegend fehlt es indes an der Durchführung eines im Anspruch genannten Verfahrensschritts im Inland.
a.
Die im Inland vorgenommenen molekularbiologischen Vorbereitungshandlungen der Beklagten für die Untersuchung in Prag begründen keine mittäterschaftliche Patentverletzung. Unstreitig findet in München eine Zellaufbereitung und eine Extraktion sämtlicher in den Proben enthaltener Nukleinsäuren statt, wie sie für molekulargenetische Untersuchungen im Allgemeinen durchgeführt wird. Das Setzen einer notwendigen und wesentlichen Bedingung für eine Patentbenutzung im patentfreien Ausland reicht gerade nicht aus. Denn die Instrumente der Mit- und Nebentäterschaft dürfen nicht dazu führen, den Tatbestand der unmittelbaren Patentverletzung auf Fälle notwendiger Teilnahme zu erstrecken, die der Tatbestand nach seinem Sinn und Zweck nicht erfassen soll (BGH GRUR 2007, 313, 314 – Funkuhr II). Im Fall eines Herstellungsverfahren kommt eine mittäterschaftliche Begehung vielmehr erst dann in Betracht, wenn einzelne anspruchsgemäße Verfahrensschritte auch im Inland durchgeführt werden (OLG Düsseldorf BeckRS 2010, 12415 – Prepaid-Karte). Dabei muss zumindest ein wesentlicher und im Anspruch niedergelegter Verfahrensschritt im Inland durchgeführt werden. Hierbei kann es sich um erfindungswesentliche Arbeiten, im Einzelfall insbesondere um die Verwirklichung einzelner, wesentlicher Merkmale eines Patentanspruchs handeln. Im vorliegenden Fall hat die Klägerin nicht aufgezeigt, dass im Inland bei Betrachtung der Mitwirkungshandlungen aller Beklagter auch nur ein einziger Verfahrensschritt vollzogen würde, durch welchen bereits ein Anspruchsmerkmal verwirklicht worden wäre. Vielmehr werden die zur Verwirklichung des Anspruchs relevanten Arbeiten unwiderlegt ausschließlich im patentfreien Ausland durchgeführt. Auch hat die Klägerin nicht widerlegt, dass die im Inland durchgeführte Extraktion sämtlicher in den Proben enthaltener Nukleinsäuren eine allgemeine molekularbiologische Tätigkeit darstellt, welche noch keinen spezifischen Bezug zu der streitgegenständlichen Erfindung hat. Insbesondere ist die Klägerin dem Vorbringen der Beklagten nicht qualifiziert entgegengetreten, dass die in Empfang genommenen Patientenproben in Deutschland lediglich unspezifisch für eine ganze Reihe verschiedener Gentests sowie zur Asservierung des Materials für eventuelle Nachforderungen von Untersuchungen aufbereitet würden. Die Klägerin führt vielmehr auf S. 23 ihrer Replik aus, diese Verfahrensschritte seien implizit in Verfahrensschritt a) – also dem Genamplifikationsschritt – des Anspruchs 1 des Klagepatents (wie aufrechterhalten) enthalten. Wie vorstehend ausgeführt, ist die Isolation der DNA indes gerade nicht Teil der Genamplifikation, denn in Anspruch 1 (2) (a) wird die Genamplifikation eines Nukleinsäurefragments beschrieben, mithin muss die DNA zum Zeitpunkt der Durchführung dieses beanspruchten Verfahrensschritts bereits isoliert worden sein.
b.
Auch die wirtschaftlich-werbenden Tätigkeiten der Beklagten begründen keine mittäterschaftliche Patentverletzung. Unstreitig bieten die Beklagten zu 1) und zu 3) zwar auf ihren Internetseiten Genuntersuchungen an. Dass dort auch explizit oder schlüssig speziell das streitgegenständliche Verfahren angeboten würde, hat die Klägerin hingegen nicht aufgezeigt.
Hinzu kommt, dass das Anbieten des Verfahrens gem. § 9 S. 2 Nr. 3 PatG nur dann verboten ist, wenn dies zur Anwendung im Inland erfolgt (vgl. auch Mes, 3. Aufl., § 9 PatG Rn. 60). Auch das geschieht vorliegend gerade nicht.
3.
Schließlich stellt das Vorgehen der Beklagten auch keine mittelbare Patentverletzung nach § 10 Abs. 1 PatG dar.
Zwar ist es gem. § 10 Abs. 1 PatG verboten, ohne Zustimmung des Patentinhabers im Geltungsbereich dieses Gesetzes anderen als zur Benutzung der patentierten Erfindung berechtigten Personen Mittel, die sich auf ein wesentliches Element der Erfindung beziehen, zur Benutzung der Erfindung im Geltungsbereich dieses Gesetzes anzubieten oder zu liefern, wenn der Dritte weiß oder es auf Grund der Umstände offensichtlich ist, dass diese Mittel dazu geeignet und bestimmt sind, für die Benutzung der Erfindung verwendet zu werden. Die Klägerin macht geltend, die Patientenproben würden Mittel darstellen, welche sich auf ein wesentliches Element der Erfindung bezögen. Sie würden mit Wissen und Wollen aller Parteien nach Prag geliefert, um diese Proben dann mit dem patentverletzenden Verfahren zu untersuchen.
Indes fehlt der doppelte Inlandsbezug. § 10 PatG verlangt insbesondere, dass das Mittel zur Benutzung der Erfindung im Inland angeboten oder ins Inland geliefert werden. Die Klägerin hat jedoch nicht vorgetragen, dass Patientenproben von den Beklagten zur Benutzung der Erfindung im Inland angeboten oder dorthin geliefert würden. Vielmehr soll die Blutprobe nach dem unstreitigen Sachverhalt gerade im patentfreien Ausland und nicht im Inland mit Hilfe des patentgemäßen Verfahrens untersucht werden.
4.
Eine alleintäterschaftliche Verantwortlichkeit der Beklagten zu 3), die der Klägervertreter in der mündlichen Verhandlung vom 06.11.2014 in den Raum gestellt hat, kann schon wegen anderweitiger Rechtshängigkeit im Verfahren 7 O 17048/12 nicht zulässiger Gegenstand dieses Rechtsstreits sein. Im Übrigen stellen auch die von der Beklagten zu 3) vorgenommenen Handlungen keine fahrlässige alleintäterschaftliche Verursachung einer Patentverletzung dar, denn die Instrumente der Mit- und Nebentäterschaft dürfen – wie ausgeführt – nicht dazu führen, den Tatbestand der unmittelbaren Patentverletzung auf Fälle notwendiger Teilnahme zu erstrecken, die der Tatbestand nach seinem Sinn und Zweck nicht erfassen soll (BGH GRUR 2007, 313, 314 – Funkuhr II). Auch insoweit muss – wie vorstehend unter Punkt 2. a. gezeigt – zumindest ein erfindungswesentlicher, beanspruchter Verfahrensschritt im Inland durchgeführt werden. Das ist vorliegend nicht der Fall. Diesbezüglich wird umfassend auf die vorstehenden Ausführungen unter Punkt 2. a. verwiesen.
C.
Die Nebenentscheidungen ergeben sich aus den §§ 91 Abs. 1, 709 S. 1 ZPO.